論文:ベンゾジアゼピン遷延性離脱症状群
Protracted Withdrawal Syndromes From Benzodiazepines PMID: 1675688
Heather Ashton
Abstract
ベンゾジアゼピン離脱症候群は、その定義と測定が非常に困難な複雑な現象である。症状の発生期間もまた定義しにくい。多くの離脱症状は、ベンゾジアゼピンに対する薬力学的耐性の結果であり、いくつかの発生メカニズムが俎上に上がっている。耐性はさまざまな脳システムで不均一に発生し、回復に時間がかかる場合がある。ベンゾジアゼピン使用中止後数週間内に発生する離脱症状は、その後何ヶ月も続く持続的な症状群と混ざって同時発症する傾向もまた見られる。遷延性離脱症状群は、必ずしも「ほんとうの("true")」薬理学的離脱症状で構成されているわけではないが、しかしそれでもベンゾジアゼピン長期使用に関連してはいる。症状には不安(ときにはベンゾジアゼピンに起因する学習能力欠如によるものも含む)、およびさまざまな感覚、運動神経症状が含まれる。ベンゾジアゼピン離脱症候群が遷延するという性質からは、ベンゾジアゼピンが中枢神経系の可逆的な機能変化を引き起こし、さらに場合によっては構造的なニューロン損傷を引き起こす可能性を示唆している。
Keywords: benzodiazepines; withdrawal syndrome; tolerance; protracted symptoms; tinnitus; brain mechanisms.
一般に、薬物離脱症候群は、薬物の初期効果の鏡像で構成される傾向がある。たとえばプロプラノロールなどのベータアドレナリン受容体拮抗薬の慢性使用からの突然の離脱は、頻脈および動悸を引き起こすことがある。高血圧薬クロニジンからの突然の離脱は、高血圧、不安、および交感神経活動の増加兆候が続くことがある。ベンゾジアゼピンも例外ではない。慢性使用後に突然中止すると、その抗けいれん効果はてんかん発作に、筋弛緩は筋肉緊張に、催眠効果は不安に置き変わることになる。ゆっくりとした退薬では、同じ症状が弱く小さく(in attenuated form)発生することになる。
しかしながら、患者にとって離脱症状のすべてが避けられないものである、というわけではない。離脱症候群の特徴とそれらの発症時間、重症度は多くの要因によって大幅に変更可能である。要因として挙げられるのは、薬物動態変数、薬物使用の投与量と期間、離脱率、原疾患(不安など)の有無、人格特性、体格、感受性、併用薬の有無、など。これらの要因がそれぞれひとつだけでは、離脱症候群の特徴を特定することはむつかしい。
ベンゾジアゼピンが主に不安や不眠に対して長期投薬されてきた事実は、離脱症候群にもっとも多い症状が不安と不眠であるという事実と相まって、さらに離脱症候群の特定をむつかしくさせている。患者がベンゾジアゼピン投与量を減少させているとき、とりわけゆっくりと減薬しているとき、突然発症した症状がほんとうに薬物関連症状(「疑似離脱」症状。Tyrer, Owen,&Dawling, 1983)なのか、それとも元々の疾患の再発なのか、離脱のストレス下にある患者の人格からの発症なのか、特定はむつかしい。このような状況で、ベンゾジアゼピン離脱症候群は主にその定義が問題になってくる。
それでもなお、高容量であれ低用量であれ治療用途でのベンゾジアゼピン使用からの離脱反応は、もはやその有無についての議論は終わっていて、ベンゾジアゼピン離脱症候群の定義と測定、そして発生率と期間を推定するために多くの試みがなされている。
Definitions and Measurements
ベンゾジアゼピン離脱中に発生する症状は、多くの研究者によってすでに説明されている(Ashton、1984、1987; Busto、Sellers、Naranjo、Cappell、Sanchez、&Sykora、1986;Hallström&Lader、1981; Murphy、Owen&Tyrer、1983、1984; Petursson &Lader、1981a、1981b; Smith&Wesson、1983; Tyrer et al。、1983; Tyrer、Rutherford、&Higgett、1981; Winokur、Rickels、Greenblatt、Snyder、&Schatz、1980; その他)。一般的な症状は図1のとおり。これらの症状はいずれもベンゾジアゼピン離脱に特有のものではない。特定の症状クラスターが特徴的に存在するが、不安に起因する精神的および身体的症状のすべてが含まれている。Owen and Tyrer(1983)およびPetursson and Lader(1981a&b)は、離脱前の不安症では珍しい、ほとんど経験しない新しい症状が、離脱時に出現することを強調している。感覚刺激(音、光、触覚、味覚、嗅覚)に対する過敏や知覚の歪み(床のうねりの感覚、動きの感覚、壁の印象、床の傾きなど)である。また、離人症、非現実化、麻痺、極度の不快気分、不安、うつ、悪心、倦怠感もまた離脱において高い確率で発生するようである(Petursson&Lader、1981a、1981b)。幻覚、身体イメージのゆがみ、精神病反応、蟻走感、筋線維束性収縮およびけいれん(ミオクローヌスに似ることもある)、大幅な体重減少などもベンゾジアゼピン離脱中に現れることがあり、不安症では珍しいものである。
Smith and Wesson(1983)とAshton(1984)は、症状において特徴的な変動に注意を向けた。それは心理的刺激がなくても症状が増減するというものである。 Smith and Wesson(1983)は、この波のような変動が、低用量ベンゾジアゼピン離脱症候群と元々の症状の再発を区別する重要なマーカーであることを示唆している。ただし、それは日内変動または数日から数週間にわたる期間内変動であったりするため、正確な記録は困難である。
ベンゾジアゼピン離脱に限った特定の症状はない。ではどのようにして症候群を定義することができるだろうか。Tyrer et al. (1981, 1983)は、プラセボ対照試験でさまざまな方法を試みた。
(1).離脱期間中に2つ以上の新しい症状が現れる。 ある研究では、知覚障害、感覚過敏症、差し迫った死の恐怖(1981)が含まれ、別の研究(1983)では、精神病症状、うつ、身体違和感、筋肉のけいれん、異常な動作、があった。離脱症状と判断するにあたって、新しい症状が最低2つある、とすることは明らかに恣意的である。
(2).主観的症状レベル(包括的精神医学的評価尺度)がベースラインの50%を超えて増加し、その後低い値に戻る。症状が消滅するかどうかは、その症状が離脱による症状か、それとも元々の疾患の再発なのかを、過剰な解釈をせずに区別する上で重要な現象である。なぜならSmith and Wesson(1983、p.88)が指摘しているように「離脱症状はいずれ治まるが、病因症状は持続する」からである。しかし、症状消滅の計測結果を、耐え難い“ほんとうの”離脱症状のため研究から脱落してしまった患者からは取得できないという事実がある。 患者の45%が1つの研究から脱落したことは注目すべきである(Tyrer et al., 1981)
(3).(1)と(2)の組み合わせ。これにより研究を終了(離脱後20週間か14週間)する前に消滅した、離脱中に発生した症状が離脱症状と定義づけられる([Tyrer et al., 1983])。Tyrer, Murphy, & Riley(1989)は、ベンゾジアゼピン離脱に比較的特有の症状について質問票を作成した。これらの症状は主に離脱期間中に発生し、離脱後にベースラインレベルに戻る。
(4).疑似離脱症状(Pseudo Withdrawal symptoms)は、患者が減薬中だと思っているところ実は服薬用量およびベンゾジアゼピン血中濃度に変化がなかったときに発生する症状として定義された。
二重盲検プラセボ対照試験から導き出されたこれらの定義は、ベンゾジアゼピン依存症、特に低用量依存症の認識に非常に役立った。しかし、特定の症状や症状クラスターの発生と重症度は、離脱症状そのもの、疑似離脱症状、および原疾患再発のさまざまなコンビネーションであるため、これらは必然的に恣意的であり大まかな定義にすぎない。
さらに、離脱前の症状との違いにフォーカスした定義では、投与量を減らしていなくとも、耐性形成によりベンゾジアゼピンを服用している間にも離脱症状が存在している可能性について考慮されていない。この状況は、比較的短時間作用型のベンゾジアゼピンで顕著に見られる。たとえば、トリアゾラムを催眠薬として服用している患者は、一般的に日中に不安(Oswald、1989)、さらには幻覚や精神病反応を発症する。症状は薬を服用することですぐに軽減され、薬をやめることで最終的には消えるのでほぼ確実に離脱症状である(Ashton、1987)。同様に、ロラゼパムとアルプラゾラム(Hermann、Brotman、&Rosenbaum、1987)では、患者はしばしば不安とパニックの増加、および投与間の渇望を発症する(Ashton、1984)。それらは、投与間に「ミニ離脱症状」を発症しているように見え、次の錠剤投与で一時的に軽減され、完全に中止すると消える。アルコールで類似の状況が見られる;アルコール依存症患者は一般に振戦や不眠症を訴える。症状はアルコールによって一時的に緩和され、断酒期間が経過すると徐々に消えていく。ジアゼパムなどの長時間作用型ベンゾジアゼピンを使用した場合でも、通常、長期使用者は不安が着実に増加し、広場恐怖症などの新しい症状が何年にもわたって発症し、服薬を継続しているにもかかわらず、知覚の歪みや離人症を伴うことがよくある。投与量の増加または別のベンゾジアゼピン追加によって一時的に緩和されることがあるが、最終的にはさらなる慢性使用中に再び現れることになり、ベンゾジアゼピンを停止した後にのみ消える(Ashton、1984、1987)。 耐性と離脱症状のメカニズムについては以下で説明するが、臨床で耐性を診断することは困難である。
こういった多くの計測不能要因により、ベンゾジアゼピン離脱症候群の境界を明確に線引きすることは厳しいと言わざるを得ない。
図1
Incidence
ベンゾジアゼピン離脱症候群の発生率は不明である。喫煙者と同様(Ashton&Stepney、1982)、ベンゾジアゼピンの数か月~数年間にわたる治療用量服薬をやめた後に通院しなくなってしまい、カウントできない人々がかなりの数いると思われる。Tyrer(1990)は、ベンゾジアゼピン減量に何の問題もない患者が多くいることのほうがむしろ驚くべきことだと述べており、一般診療でのベンゾジアゼピン離脱症候群の発生率は約30%だろうとしている(Tyrer et al., 1981、1983; Tyrer, 1989; Tyrer, Murphy, &Riley, in press; Tyrer, 1990)。一方、専門治療に紹介された患者では、発生率は100%になるようだ(Ashton, 1987; Lader&Olajide, 1987; Petursson&Lader, 1981a)。健康な実験対象者や、スポーツ傷害でベンゾジアゼピンを処方されたような元々不安症状を抱えていなかった患者でも、反跳性不眠(Kales、Scharf、&Kales、1978)やその他の一般的なベンゾジアゼピン離脱症状が発生している(Lader, 1988)。さらに、妊娠中に「治療用量」のベンゾジアゼピンを服用していた母親の新生児でベンゾジアゼピン離脱症候群の発生が報告されている(Rementeria&Bhatt、1977)。
当然のことながら、ベンゾジアゼピン離脱反応の発生率は、選択された患者母集団だけでなく測定基準にも左右される。Tyrer et al(1983)の研究では、離脱(1)と(2)(上記を参照)の定義をそれぞれ単独で採用した場合、疑似離脱反応の発生率は約20%であった。組み合わ定義(3)(上記を参照)では、「ほんとうの」離脱症状の発生率は44%であり、疑似離脱反応はなかった。もちろんこの発生率は、研究への参加に同意し研究を首尾よく終了できた患者群だけで計測されたものである。離脱中に脱落したり、離脱を完了することをあきらめた対象群はカウントしていない(Tyrer et al.,1981の研究における適格対象患者のうち45.5%が脱落)。したがってベンゾジアゼピン離脱の発生率は、その診断と同様に、やはりベンゾジアゼピン離脱症候群の定義の問題になってくる。
Duration
このようにベンゾジアゼピン離脱症候群の診断は困難である。そしてその継続期間を推測することはさらに困難になってくる。ほとんどの推定が約5〜28日程度で、重症度のピークは離脱後約2週間、その後ほとんどの症状は離脱前のレベルに戻るとしている(Busto et al., 1986; Murphy et al., 1984; Owen&Tyrer, 1983; Petursson&Lader, 1981a, 1981b; Tyrer et al., 1981,1983)。
こうした症状持続期間に関する調査は、研究が患者を調査しつづける期間におおいに左右されるだろうし、実際いくつかの研究が離脱後長期にわたって遷延するベンゾジアゼピン離脱症状の特徴に注目してきた。たとえば、Smith and Wesson(1983)は低用量ベンゾジアゼピンから離脱した後、症状が完全に治まるまでに通常6〜12か月かかることを観察した。長期にわたる症状には、不安、不眠、知覚異常、感覚変化、筋けいれん、精神病様症状などがあった。Ashton(1984、1987)は、同様の長期遷延性を報告した。Tyrer(1990)は、離脱後6か月の「遷延性離脱症候群」について言及している。Hallström and Lader(1981)は、うまく離脱できた患者が“ふつうの生活に戻った”後、その患者の数か月間を観察してみたところ、ハミルトン不安スコアがその後もずっとベースラインレベルを上回っていることを発見した。Olajide and Lader(1984)は、うつはベンゾジアゼピン離脱症候群のひとつとして必ず存在し、感受性の高い人では離脱後数ヶ月続く可能性があることを示唆した。この現象はAshton(1987)によっても観察された。Busto, Fornazzari and Naranjo(1988)は、重度の耳鳴りがベンゾジアゼピン離脱中に最初に発生し、中止後6か月~12か月継続した後、最終的には減少または消失した2つの症例について述べている。この2つの症例のうちひとつで、離脱から6か月後に1週間超の二重盲検プラセボ対照試験の中で使用したジアゼパムによって耳鳴りが緩和された。そしてつづく6か月間の断薬中に耳鳴りは徐々に認容可能となっていった。
6週間かけてベンゾジアゼピンから離脱し、その後4週間追跡調査した68人の患者を対象とした最近の研究(Tyrer etal.1989)では、個々の症状によってそのピークがさまざまなであることがわかった(自己評価スケールを使用)。症状の一部(うつ、めまい、麻痺、非現実感)の平均スコアは早期にピークに達したが、いっぽうでその他の症状(悪心、記憶障害、浮動性めまい、触覚過敏、運動障害)の平均スコアは離脱から8週間後に最大となった。ただし、個々の患者ごとのスコアは報告されておらず、30%が研究から離脱している。これらの所見は、一般的な離脱症状期間と見なされる5〜28日を超えてもまだ症状が持続することを示唆している。
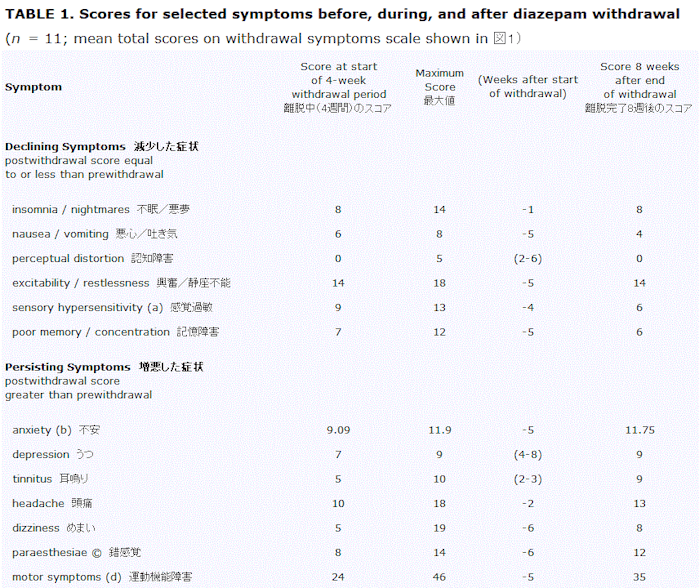
Ashton, Rawlins and Tyrer(1990)は、図1に示す評価尺度を使用して、二重盲検プラセボ対照条件下でジアゼパム離脱症状を発症した患者を記録した。離脱は4週間かけて行われ、離脱完了から8週間後まで患者の状態を追跡調査した。患者の半数はプラセボを投与され、残りの半数は離脱症状を示した。離脱に成功したプラセボ群12人の患者のうち11人の選択された症状の時間経過の分析を表1に示す。離脱完了から8週間後の頭痛、めまい、うつ、耳鳴り、麻痺および運動障害の平均スコアは離脱前よりも高いままであった。他の症状は消滅はしなかったが減少した。この調査結果から、ベンゾジアゼピン離脱後の症状の持続期間が数週間ではなく数ヶ月であることが多いことを再び示している。またTyrer et al.(1989)とAshton et al.(1990)の研究では、サンプル群の規模、選択対象そして離脱率が異なるものの、さまざまな別の症状がやはり持続することがわかっている。それらが「ほんとうの」ベンゾジアゼピン離脱症状であるのかどうか、は不明である。
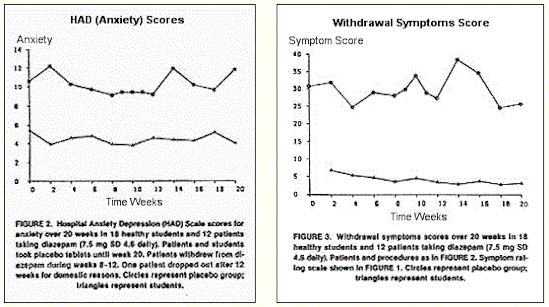
離脱症候群の期間を評価する際のさらなる問題は、ベースライン(離脱前)の症状と不安スコアの解釈である。ベンゾジアゼピン離脱症状を呈している患者は、しばしば高レベルの不安と多くの精神的および身体的症状を示している。図2と図3は、Hospital Anxiety Depression(HAD)(Zigmond&Snaith、1983)と、ベンゾジアゼピンを服用している12人の患者の症状評価スコアを、18人の健康な大学生の期末試験直前のスコアと比較して示したもの。両グループはプラセボ錠剤を服用し、20週間追跡調査された。ベンゾジアゼピン服用患者群は8週~12週かけてベンゾジアゼピンから離脱した。ベンゾジアゼピン服用患者がまだ減薬を開始していない研究開始時ですら、すでに正常な被験者よりかなり高いスコアとなっていることがわかる。
あきらかにベンゾジアゼピン服用患者においては、ベンゾジアゼピンは不安を効果的に制御しておらず、上記で述べたように症状群の少なくとも一部が薬物投与下でも、耐性を形成したことによる「離脱」症状であった可能性がある。症状は離脱後に消滅すると予想されるが、時間がかかる可能性がある。中止後8週間でベースラインレベルを下回るというエビデンスはないが、残念ながら(ほとんどの研究において)正式なアセスメントは8週間で終了となった。しかしながら、患者との継続的な臨床的接触において、不安症状が時間とともに減少していくことを示した。このゆっくりとした改善は、症状が離脱後何ヶ月もかけて徐々に改善するという上記の観察(Ashton. 1984, 1987; Busto et al., 1988; Hallström&Lader, 1981; Olajide and Lader, 1984; Smith&Wesson, 1983)を裏付けている。何人かは離脱前の数年にわたる機能不全状態から、離脱後通常の生活を再開することができた。
これら長期的な症状のどれが「ほんとうの」薬物離脱反応であろうか?ベンゾジアゼピン離脱症候群が終了する時期を正確に特定し、残存症状が他の要因によるものであると確実に言うことは可能であろうか?この問題はインフルエンザまたは伝染性単核球症で発生した症状に関わった要因を特定することと似ている。ウイルス性中毒症の影響のみであろうか?ウイルスの影響の結果として生じる二次細菌感染も含まれているだろうか?ベンゾジアゼピン離脱症状のように、感染後に何か月も発症する無気力やうつもまた関連要因に含まれるだろうか?もう一度述べるが、ベンゾジアゼピン離脱症候群はどうしても定義の問題に戻される。中枢神経伝達の薬物誘発性摂動は、個々の、遺伝的に決定された、脳活動の学習パターンに融合しているため、ベンゾジアゼピン離脱症状持続時間の明確な定義はおそらく不可能である。
表1
図2と図3
Protracted Symptoms After Benzodiazepine Withdrawal
以上に述べた定義の問題は、長期遷延性離脱症候群を説明しようとする場合、さらにその重要性が増してくる。ベンゾジアゼピン離脱後もその患者を長期間観察している者は、一部の患者において特定の症状が非常に長い間持続することに必ず驚かされるはずである。これらは「ほんとうの」ベンゾジアゼピン離脱症状ではない可能性がある。 それでもなお、それらはやはりベンゾジアゼピン使用におそらく関連しており、しばしば臨床上の問題を提示する。個人的な観察や他の報告から、ベンゾジアゼピン離脱後の一般的と思われるいくつかの長期症状例を以下にリストする。残念ながら、ベンゾジアゼピン治療を受けていない患者における以下の症状の発生率と持続期間、それに相対するベンゾジアゼピン離脱患者における以下の症状の発生率と持続期間、に関する利用可能なデータはない。また、どの患者が特に脆弱であるかを示す既知の予測因子もない。
不安:不安はベンゾジアゼピン離脱後何ヶ月も続く可能性があるが、1〜2年後には離脱前のレベルをゆっくりと下回る(Ashton、1987)。消滅が遅い理由の1つは、ベンゾジアゼピンがストレス対処戦略の学習を阻害することである。これは動物とヒトで実証されている(Gray、1987)。その結果、ベンゾジアゼピン離脱後も、患者がストレスの多い状況に対処する能力が低下しつづける(Ashton、1989; Murphy&Tyrer、1988; Owen&Tyrer、1983)。新たに自然のストレス制御戦略を学習するには、外因性薬物をもってしてストレス対処してきた年数と同じ期間が必要かもしれない。
したがって、ベンゾジアゼピン離脱後も不安が続くことは、必ずしもベンゾジアゼピン治療前に存在していた不安状態の再発を意味するわけではない。つまり、ベンゾジアゼピンを長期使用していたことによる学習不全を露呈した、という可能性がある。ベンゾジアゼピン服用者は、特性不安スコアが高い傾向があり(Ashton and Golding、1989; Golding&Cornish、1987; Golding、Harper、&Brent-Smith、1983)、離脱症状のストレスに特定の脆弱性が加わっている可能性がある。治療がなくとも、広場恐怖症やパニックなどの遷延性不安症状はベンゾジアゼピン離脱後に徐々に解消することはあるが(Ashton、1987)、行動療法によって回復プロセスが早まる可能性はある。
うつ:うつは、ベンゾジアゼピン慢性使用によって引き起こされたり悪化したりすることがあるが(Lader&Petursson、1981)、離脱症候群のひとつでもあるようだ(Olajide&Lader、1984)。それは大うつ病性障害として診断できるほど十分に重症になり得(Ashton、1987)、数ヶ月間続くかもしれない。Olajide and Lader(1984)は、離脱後うつのメカニズムは中枢性セロトニンの枯渇であることを示唆しているが、これに関する直接的なエビデンスはない。臨床的には、うつ症状は一般的なうつ病と同じであり抗うつ薬に反応する。離脱うつ症状がうつ病の病歴のある患者でより一般的に現れるものなのか、またそれが離脱してから数年後に再発するものなのか、は明らかでない。
耳鳴り:耳鳴りは一般的なベンゾジアゼピン離脱症状のひとつであり、感覚刺激に対する最初で特徴的な神経過敏に起因すると思われる。 通常、数週間で消滅するが、遷延性離脱症状群と言えるほど長引くこともある。Busto et al(1988)は、耳鳴りが離脱後6か月と12か月持続した2つの症例について、そして重度の耳鳴りのためにベンゾジアゼピンから離脱できなかった患者についてひとつの症例で説明している。個人的に臨床で観察した遷延性耳鳴り症状患者を以下にいくつか記述する。
ケース1:女性、54歳。ベンゾジアゼピン使用期間:8年。 1986年にオキサゼパム45mg/日をゆっくりと減薬して離脱。右側の耳鳴りは以前離脱を試みた時に最初に気づく。最終的に離脱後、重症になり、2年後も常に鳴っていて重症。主に片方だけ。頭蓋骨X線、CATスキャン、EEG、耳鼻咽喉科の検査ではわずかな両側性(対称性)の高音性失音を除いて、異常は検出さず。臨床的に不安症や抑うつではない。他のすべての離脱症状はすぐに消滅した。薬の服用はない。
ケース2:女性、62歳。ベンゾジアゼピン使用期間:18年。 1988年にジアゼパム15mg/日からゆっくりと減薬して離脱。両側性耳鳴りは、以前離脱を試みた時に最初に気づく。最終的に離脱後、重症になり、1年後も常に鳴っていて重症。耳鼻咽喉科の検査:中等度の両側性先天性失音症;補聴器を装着している。臨床的に不安症や抑うつではない。他の離脱症状はない。服薬なし。
ケース3:女性、58歳。ベンゾジアゼピン使用期間:20年。 1988年に4週間にわたってジアゼパム20mg/日を減薬、そして中止。急性精神病反応を発症、1週間で消滅。離脱から1ヶ月後に左側耳鳴り発生。 3か月後耳鳴りが絶え間なく続いたため、ジアゼパム20mg/日を再開したがわずかな改善しか見られず。 1988~1989年の1年間かけて2回目の離脱。離脱中はずっと重度で、断続的ではあるが左側耳鳴りが持続する。耳鼻咽喉科の検査では、わずかな両側性(対称性)の先天性失音を除いて陰性。投薬:ミアンセリン30mg/日を耳鳴りの発症後に開始。カルバマゼピンを最近追加しがた耳鳴りには効果なし。
ケース4:女性、70歳。ベンゾジアゼピン使用期間:20年。 1985年にフルラゼパム30mg/日から離脱したときに主に右側の耳鳴り発生。それ以来耳鳴りは継続し、一定期間のジアゼパム投与でも軽減されず。耳鼻咽喉科検査は正常。薬:向精神薬なし、喘息の吸入器。
耳鳴りはかなり一般的であり、ベンゾジアゼピン使用と明らかな関連性があることは偶発的かもしれない。しかしこれらのケースは、ベンゾジアゼピンが時折永続的または非常にスローな可逆的脳損傷を引き起こす可能性があるという疑惑を引き起こす。このような損傷は、CATスキャンでは検出できないであろう。ある研究(Lader&Petursson、1984)は、慢性ベンゾジアゼピン使用者の軽度の皮質収縮を示唆したが、後の研究(Perera、Powell、&Jenner、1987)ではそれは確認されなかった。 上記の患者のうちの2人は片頭痛を訴えていた。
知覚異常:知覚異常は、うずき、チクチク(pins and needles)、四肢や周囲領域のしびれといった症状であり、これもまた一般的なベンゾジアゼピン離脱症状のひとつである。不安神経症でも発生するもので、おそらく過呼吸が原因である。ベンゾジアゼピンは、二酸化炭素に対する呼吸中枢の感受性を低下させ(Gilmarti, Corris, Stone, Veale, &Gibson, 1988)、離脱中に呼吸中枢が過敏になり、過呼吸を引き起こす可能性がある。知覚異常は通常、離脱から数週間以内に消滅する。 しかし時折、数ヶ月から数年に及ぶ指、足、および脚のしびれや灼熱感を訴える患者もいる。症状は末梢感覚神経障害を示しており、軽い接触に対して明らかな過敏反応を示す場合がある。 以下の二つの症例は、ベンゾジアゼピン離脱クリニックで個人的に観察できた典型的なケースである。
ケース1:女性、56歳。ベンゾジアゼピン使用期間:15年。 1984年にロラゼパム7.5mg/日から1.5mg/日まで減薬中に足の重度灼熱痛発生、その後継続。ジアゼパムに置換し1987年から1988年にかけてゆっくりと離脱。灼熱痛はさらに1年間続き、徐々に強度が低下し、今ではほとんど消滅。異常兆候はなし。周辺パルス良好。投薬; 1988年からプロメタジン50mg。
ケース2:女性、67歳。ベンゾジアゼピン使用期間:12年。 1981年にメダゼパムを15mg/日から5mg/日まで減薬中に、足と脚に激しい火傷様灼熱痛が発生。 1985年ジアゼパム置換後にゆっくりと離脱。その間痛みは持続。1986年:クロルジアゼポキシド投与で緩和されず、依然として脚の激しい灼熱痛。 1989年:痛みはまだ残っている。神経学的検査、神経伝導検査、血清葉状体およびB12レベルは正常。周辺パルスが存在し、正常。
蟻走感もまた一般的なベンゾジアゼピン離脱症状のひとつである。多くの患者が、ときおり昆虫が皮膚を這う感覚やシラミが髪の毛の中にいる感覚を訴える。スライムや水が体の上を流れる感覚、内部の振動感、「内部が震える」感覚など、より奇妙な感覚が報告され、これらの症状が長期間持続することがある。このような症状は、上記の灼熱感の変種であるかもしれないし、精神病であるかもしれない。だがその発生はベンゾジアゼピン離脱と時間的におおいに関連性がある。
運動機能症状:筋緊張の増加、反射亢進、振戦、線維束性収縮、および筋けいれんはベンゾジアゼピン離脱の一般的な特徴であり、通常は数週間以内に消滅する。時折、筋けいれんが離脱後1年以上続くことがあり、臨床像はミオクローヌス、チック、過剰驚愕反応を示している場合がある。通常は肩甲帯と四肢の筋肉が影響を受けるが、眼瞼痙攣が発生する場合もある。一部の患者が、睡眠開始時に全身の激しいけいれんを訴え、これは一夜に20回以上発生したりする。むずむず脚症候群も長期持続する可能性がある。プロプラノロールによって改善される症状が多いため、末梢交感神経緊張の増幅に起因するのかもしれない。その他の症状は中枢的に発生し、部分的にカルバマゼピンに反応する可能性がある。眼瞼痙攣は、3か月間隔でボツリヌストキシンを局所注射することで制御できる。こういった遷延性運動機能症状あるということは、ベンゾジアゼピンが運動ニューロンまたは中枢運動経路の長期的な過興奮を引き起こしている可能性が高い。
胃腸症状:胃腸症状は、ベンゾジアゼピンの慢性的な使用中および離脱中に非常に一般的である。多くの慢性ベンゾジアゼピン使用者が胃腸科医によって検査され「過敏性腸症候群」であることがわかった(Ashton、1987)。胃腸症状は過呼吸によって悪化する可能性があり(Lum、1987)、何年も「過敏性腸症候群」を患っていたにもかかわらず、ベンゾジアゼピン離脱後に完全にそれが消失する患者がいる。それでもなお、離脱中に発症し離脱後も何ヶ月も持続する離脱後食物不耐性とガス状の腹部膨満を訴える患者は一定数いる。特定食物アレルギーの検査はほとんどの場合陰性であり、従来の治療は効果がない。患者はしばしば代替療法や「フリンジ」療法に走り、さまざまな食事療法を行い、腸のカンジダ症や免疫系の問題であると信じるようになるが、この主張は科学的裏付けがない。Lum(1987)は、過呼吸がヒスタミン放出を引き起こし、慢性過換気者は食物不耐性と偽アレルギー反応の発生率が高いと報告している。胃腸機能およびコリオコステロイドと免疫反応(ストレスの影響を受けることが知られている)に対するベンゾジアゼピン離脱の影響は、もっと注目されてもよい。
Brain Mechanisms of Benzodiazepine Withdrawal Symptoms
ベンゾジアゼピンの主な効果は、脳内のシナプス後GABA-A受容体に対するガンマアミノ酪酸(GABA)作用の増強である。この効果は、GABA受容体複合体の特定のベンゾジアゼピン結合部位との相互作用に起因して起こるもので(Möhler&Okada、1977; Squires&Braestrup、1977)、受容体に対するGABA親和性を高める(Costa、1981)。GABAニューロンは、局所回路を形成する小さな介在ニューロンで構成されており、空間ドメインを通過する他ニューロンの興奮性に強力な影響を及ぼす(Bloom、1985)。このような局所GABA回路は、網様体、大脳辺縁系構造、大脳皮質、小脳皮質など、脳全体に広く分布している(Young&Kuhar、1980)。 GABAは神経活動の普遍的な阻害剤であり、興奮性神経伝達物質の放出も阻害する(Benton&Rick、1976)。したがって、多くの脳部位でのGABA作用の増強だけがベンゾジアゼピンの影響というわけではでなく、アセチルコリン、ノルアドレナリン、ドーパミン、およびセロトニンの放出減少も含まれる(Faefely、Pieri、Pole、and Schaffer、1981)。ベンゾジアゼピンの臨床効果は、重要な部位において、こういった一次効果と二次効果の組み合わせによって起きるものである。たとえば抗不安作用は、中隔海馬経路におけるセロトニン作動性およびノルアドレナリン作動性活性を低下させるといったようなもの(Gray、1981)。このように、ベンゾジアゼピンの作用は、特定の神経伝達物質や脳の経路に限定されるものではない。
薬物の慢性的な使用によって、正常機能を回復させようとする恒常性反応が徐々に生じるようになる。つまり、ベンゾジアゼピンを慢性的に使用することでGABA受容体に代償性の変化が起きてくる。親和性が変化し受容体密度が低下し、結果としてGABAに対するGABA受容体の感度が低下するのである(Cowan&Nutt, 1982; Nutt, 1986)。加えて、GABAによって制御される二次システムもまた変化するため、薬物使用下にあっても興奮性神経伝達物質の出力が回復していき、および/または、興奮系受容体の感度が増加する。一次変化と二次変化の合わせ技によって、最終的にベンゾジアゼピン耐性をもたらすわけである。
この薬力学的耐性は、さまざまなベンゾジアゼピン効果に対して不均一に発生する。たとえば、耐性は抗不安作用よりも催眠作用、および抗けいれん作用に対してより迅速に現れる(Sepinwall&Cook、1979)。耐性形成の対象となるベンゾジアゼピン効果は、個人間で異なるであろう。これはおそらく、脳のさまざまな部分において内因性GABA作用が違うことが原因で、翻ってそれが人格特性とストレス感受性に反映される。耐性は決して完全ではなく、おそらくすべての脳系で完全な平衡に達することはない。これは慢性ベンゾジアゼピン使用者の耐性形成率が高い理由の1つになる(Ashton、1987)。特に催眠効果に対する急性耐性は急速に現れるが、慢性耐性は数週間かけて形成される。慢性耐性が一旦形成されると、それはアルコール(Cicero、1979)やベンゾジアゼピンなど中枢神経系抑制剤の中止後に、数ヶ月または数年も続く可能性がある。
薬力学的耐性の形成によって、離脱症候群の舞台がととのうわけである。薬物の中止は、薬物の存在を打ち消すために生じたすべての恒常性適応を露呈させる。結果として、多くの神経伝達物質とその受容体そしてさまざまな脳系活動は、もはやベンゾジアゼピンという抑制を失うことで、リバウンドという形で解放される。臨床的にはこの状態は離脱症候群として現れる。症状群は、薬物によって最初に誘発された効果とはほとんど正反対のもので構成されている。症状の範囲、期間、および重症度は、適応変化を受けたシステムや適応変化の大きさ、そして薬物離脱速度によって左右される。一部の著者はリバウンドと離脱を区別しているが、そのメカニズムは同じである (Lader, 1988)。急性離脱反応は、適切な用量の薬剤投与によって逆転し、離脱前の状態を回復する。
恒常性変化がゆっくりと逆転するにつれ、離脱症状は減少していく。そのプロセスは、必ずしもすべてのシステムで均等に進行するわけではない。 Tyrer(1989)and Ashton et al(1990)(表1)によって示されたベンゾジアゼピン離脱中におけるそれぞれの症状の出現時間と持続時間はその不均一なプロセスを表現しているのかもしれない。ベンゾジアゼピンによって誘発された脳機能の混乱は非常に複雑であり、あまりにも症状が多くそしてそれらが変動することはとくに驚くべきことでもない。さまざまな症状はAshton(1984)によって示唆されているように、さまざまな神経伝達物質システム間のバランスの乱れを反映していて、個人の特性や感受性に応じて大きな個人差を示すからだ。今まで述べてきたとおり、離脱症候群の終了に明確な時間制限を設定することは困難である。一般的には数週間で低下するが、場合によっては1年以上続くこともある(Cicero、1979)。非常にゆっくりな逆転プロセスが長期遷延性離脱症状群の原因であると思われる。
ベンゾジアゼピンによって誘発される変化は、永続的であるかもしくは非常にスローな可逆性であると思われる。ベンゾジアゼピンはストレス対処戦略の学習をあきらかに阻害するため(Gray、1987)、長期使用後に中止すると、特にストレスに対処する能力が欠如していることを露呈するかもしれない。これにより遷延性の不安症状やうつとして持続する可能性がある。新しい学習が適切なシナプス変化を誘発し、かつ内因性GABA作用変化をもたらすまで、不安症状はつづくかもしれない。
最後に、ベンゾジアゼピンが構造的な神経学的損傷を引き起こす可能性があるかどうかという疑問が残る。アルコールと同様、ベンゾジアゼピンは脂溶性であり、脳に高濃度であり、大脳皮質、小脳、および大脳辺縁系の機能を損なう。何年にもわたって使用すると、部分的にしか回復しない皮質の収縮などの物理的変化を引き起こす可能性がある。物理的変化は、アルコール依存症者であればCATスキャン研究(Lee, Möller, Hardt, Haubek & Jenson, 1979; staff, British Medical Journal, 1981)によって実証されているが、慢性ベンゾジアゼピン使用者では決定的ではない(Lader&Petursson, 1984; Perera , Powell, & Jenner, 1987)。ただし、このような手法では微妙な変化を検出するのに十分ではないだろう。知的機能の標準テストもまた、離脱後にも持続する一部の患者の軽度認知障害を検出するのに十分ではない。一部の長期にわたるベンゾジアゼピン離脱症状(耳鳴りやその他の神経学的および心理学的症状を含む)は、物理化学的神経損傷に起因する可能性がある。
これらの症状は、ベンゾジアゼピン使用を再開しても完全には軽減されない。ベンゾジアゼピン離脱にはまだ多くの不可解な特徴があり、ベンゾジアゼピンのストーリーは未完成のままである(Ashton、1984)。
References
Ashton, H. (1984). Benzodiazepine withdrawal: An unfinished story. British Medical Journal, 288, 1135-1140.
Ashton, H. (1987). Benzodiazepine withdrawal: Outcome in 50 patients. British Journal of Addiction, 82, 665-671.
Ashton, H. (1989). Risks of dependence on benzodiazepine drugs: A major problem of long-term treatment. British Medical Journal, 298, 103-104.
Ashton, H., & Golding. J.F. (1989). Tranquillisers: Prevalence, predictors and possible consequences. Data from a large United Kingdom Survey. British Journal of Addiction, 84,541-546.
Ashton, H., Rawlins, M.D. & Tyrer, S.P. (1990). A double blind placebo controlled study of buspirone in diazepam withdrawal in chronic benzodiazepine users. British Journal of Addiction, 157, 232-238.
Ashton, H., & Stepney, R. (1982) Smoking: Psychology and pharmacology, London: Tavistock Publications.
Benton, D., & Rick, J.T. (1976). The effect of increased brain GABA produced by amino-oxyacetic acid on arousal in rats. Psychopharmacology, 49, 85-89.
Bloom, F.E. (1985). Neurohumoral transmission in the central nervous system. In A.G. Gilman, L.S. Goodman, T.W. Rall, & F. Muland (Eds.), The pharmacological basis of therapeutics (pp. 236-259). New York: Macmillan.
Busto, U., Fornazzari, L., & Naranjo, C.A. (1988). Protracted tinnitus after discontinuation of long-term therapeutic use of benzodiazepines. Journal of Clinical Psychopharmacology, 8, 359-362.
Busto, U., Sellers, E.M., Naranjo, C.A. Cappell, H.P., Sanchez, C.M., & Sykora, K. (1986). Withdrawal reaction after long-term therapeutic use of benzodiazepines. New England Journal of Medicine, 315, 654-659.
Cicero, T.J. (1979). Tolerance to and physical dependence on alcohol: Behavioural and neurobiological mechanisms. in Brain and pituitary peptides (pp.1603-1617). Munich: Ferring Symposium 1979.
Costa, E. (1981). The role of gamma-aminobutyric acid in the action of 1,4 benzodiazepines. In J.W. Lamble (Ed), Towards understanding receptors (pp. 176-183). Amsterdam: Elsevier/North Holland.
Cowen, P.J., & Nutt, D.J. (1982). Abstinence symptoms after withdrawal from tranquillising drugs: Is there a common neurochemical mechanism? Lancet,2,360-362.
Gilmartin, J.J., Corris, P.A., Stone, T.N., Veale, D., & Gibson, G.J. (1988). Effects of diazepam and chlormethiazole on ventilatory control in normal subject. British Journal of Clinical Pharmacology, 25, 766-770.
Golding, J.F., & Cornish, A.M. (1987). Personality and life-style in medical students: Psychopharmacological aspects. Psychology and Health, 1, 287-301.
Golding, J.F., Harper, T., & Brent-Smith, H. (1983). Personality, drinking and drug-taking correlates of cigarette smoking. Personality and Individual Differences, 4, 703-706.
Gray, J.A. (1981). Anxiety as a paradigm case of emotion. British Medical Bulletin, 37, 193-197.
Gray, J. A. (1987). The neuropsychology of emotion and personality. In S.M. Stahl, S.D. Iverson, & E.C. Goodman (Eds.), Cognitive neurochemistry (pp.171-190). Oxford: Oxford University Press.
Haefley, W., Pieri, L., Pole, P., & Schaffer, R. (1981). General pharmacology and neuropharmacology of benzodiazepine derivatives. In H. Hoffmeister, and G. Stille (Eds.), Handbook of experimental pharmacology (Vol. 55, 11, pp. 13-262). Berlin: Springer-Verlag.
Hallström, C., & Lader, M. (1981). Benzodiazepine withdrawal phenomena. International Pharmacopsychiatry, 16, 235-244.
Hermann, J.B., Brotman, A.W., & Rosenbaum, J.F. (1987). Rebound anxiety in panic disorder patients treated with shorter-acting benzodiazepines. Journal of Clinical Psychiatry, 48 (suppl. 10), 22-28.
Kales, A., Scharf, M.B., & Kales, J.D. (1978). Rebound insomnia: A new clinical syndrome. Science, 201, 1039-1041.
Lader, M. (1988). The psychopharmacology of addiction - Benzodiazepine tolerance and dependence. In M. Lader (Ed.), The psychopharmacology of addiction (pp. 1-14). Oxford: Oxford University Press.
Lader, M.H., & Olajide, D. (1987). A comparison of buspirone and placebo in relieving benzodiazepine withdrawal symptoms. Journal of Clinical Psychopharmacology, 7, 11-15.
Lader, M.H., & Petursson, H. (1981). Benzodiazepine derivatives - Side effects and dangers. Biological Psychiatry, 16, 1195-1212.
Lader, M.H., Ron, M., & Petursson, R.H. (1984). Computed axial brain tomography in long-term benzodiazepine users. Psychological Medicine, 14, 203-206.
Lee, K., Moller, L., Hardt, F., Haubek, A., & Jenson, E. (1979). Alcohol-injured brain damage and liver damage in young males. Lancet 2, 759-761.
Lum, L.C., (1987). Hyperventilation syndromes in medicine and psychiatry: A review. Journal of the Royal Society of Medicine, 80, 229-231.
Möhler, H., & Okada, T. (1977). Benzodiazepine receptors: Demonstration in the central nervous system. Science 198, 849-851.
Murphy, S.M., Owen, R.T., & Tyrer, P.J., (1984). Withdrawal symptoms after six week’s treatment with diazepam. Lancet, 1389.
Murphy, S.M., & Tyrer, P. (1988). The essence of benzodiazepine dependence. (pp. 157-167). Oxford: Oxford University Press.
Nutt, D. (1986). Benzodiazepine dependence in the clinic: Reason for anxiety? Trends in Pharmacological Sciences 7, 457-460.
Olijade, D., & Lader, M. (1984). Depression following withdrawal from long-term benzodiazepine use: A report of four cases. Psychological Medicine, 14, 937-940.
Oswald, I. (1989) Triazolam syndrome 10 years on. Lancet 1, 451-452.
Owen, R.T., & Tyrer, P. (1983) Benzodiazepine dependence: A review of the evidence. Drugs, 25, 385-398.
Perera, K.M.H., Powell, T., & Jenner, F.A. (1987). Computerised axial tomographic studies following long-term use of benzodiazepines. Psychological Medicine, 17, 775-777.
Petursson, H., & Lader, M.H. (1981a) Withdrawal from long-term benzodiazepine treatment. British Medical Journal, 283, 634-635.
Petursson, H., & Lader, M.H. (1981b). Benzodiazepine dependence. British Journal of Addiction, 76, 133-145.
Rementeria, J.L., & Bhatt, K. (1977). Withdrawal symptoms in neonates from intrauterine exposure to diazepam. Journal of Paediatrics, 90, 123-125.
Sepinwall, J., & Cook, L. (1979). Mechanisms of action of the benzodiazepines: Behavioural aspects. Federation Proceedings 39, 3024-3031.
Smith, D.E., & Wesson, D.R. (1983). Benzodiazepine dependency syndromes. Journal of Psychoactive Drugs, 15, 85-95.
Squires, R.F., & Braestrup, C. (1977). Benzodiazepine receptors in the rat brain. Nature, 266,732-734.
Staff. (1981). Minor brain damage and alcoholism. British Medical Journal, 2, 455-456.
Tyrer, P. (1990) Diagnosis of benzodiazepine dependence. Unpublished manuscript.
Tyrer, P., Murphy, S., & Riley, P. (1989). The benzodiazepine withdrawal symptom questionnaire. Journal of Affective Disorders, 19, 53-61.
Tyrer, P., Owen, R., & Dawling, S. (1983). Gradual withdrawal of diazepam after long-term therapy. Lancet 1, 1402-1406.
Tyrer, P., Rutherford, D., & Higgett, T. (1981). Benzodiazepine withdrawal symptoms and propranolol. Lancet, 1, 520-522.
Winokur, A., Rickels, K., Greenblatt, D.J., & Schatz, N.J. (1980). Withdrawal reaction from long-term low dosage administration of diazepam. Archives of General Psychiatry, 37, 101-105.
Young, W.S., & Kuhar, M.J. (1980). Radiohistochemical localisation of benzodiazepine receptors in rat brain. Journal of Pharmacology and Experimental Therapeutics, 212, 337-346.
Zigmond, A.S., & Snaith, R.P. (1983). The hospital anxiety and depression (HAD) scale. Acta Psychiatrica Scandinavica, 67, 361-370.
(翻訳:ベンゾジアゼピン情報センター 管理人)
著者:Heather Ashton

英国ニューカッスル大学臨床精神薬理学名誉教授。
1951年オックスフォード大学卒業、生理学学位(BA)を取得。1954年医学資格(BM、BCh、MA)を取得。1956年に医学博士(DM)を取得。1958年MRCP(Member of the Royal College of Physicians, London)、1975年にFRCP(Fellow of the Royal College of Physicians, London)に選出される。
1975年から国民保健サービスの臨床精神薬理学専門医。1994年から国民保健サービスの精神医学専門医。
1965年以来、ニューカッスル大学で研究員(講師、上級講師、教授)および臨床医として、最初は薬理学部、後に精神科に勤務。おもな研究は向精神薬(ニコチン、大麻、ベンゾジアゼピン、抗うつ薬など)が人間の脳と行動に及ぼす影響について。生涯で約250の論文を発表し、そのうち50超がベンゾジアゼピンに関するもの。喫煙、大麻、ベンゾジアゼピンに関するさまざまな政府委員会にエビデンスを提供してきた。
2019年9月15日没